
CER Groupe réalise des études de toxicologie, de sécurité et des études cliniques pour les médicaments vétérinaires, en parfaite conformité avec les exigences de la VICH et du CVMP.
Études à vocation réglementaire pour la santé humaine, la santé animale, les dispositifs médicaux et les produits bioactifs
Vous recherchez un partenaire BPL de confiance pour générer des données de sécurité non cliniques robustes pour votre produit ?
CER Groupe est certifié BPL par l'autorité compétente belge (Sciensano) depuis 1993, avec un périmètre de toxicologie BPL dédié depuis 2010.
Études réalisées
Certifié BPL depuis 1993
Semaines d’introduction de l’étude
CER Groupe réalise des études de toxicologie et de sécurité conformes aux Bonnes Pratiques de Laboratoire (BPL). Toutes les études de toxicologie in vivo sont conçues conformément aux lignes directrices ICH, VICH, OCDE et ISO, avec un fort accent sur la pertinence scientifique, le bien-être animal et l'acceptation réglementaire. La durée des études, les niveaux de doses, la taille des groupes et les paramètres sont définis en fonction de l'usage clinique ou réglementaire prévu, garantissant des données à la fois adaptées à leur finalité et prêtes pour les inspections.
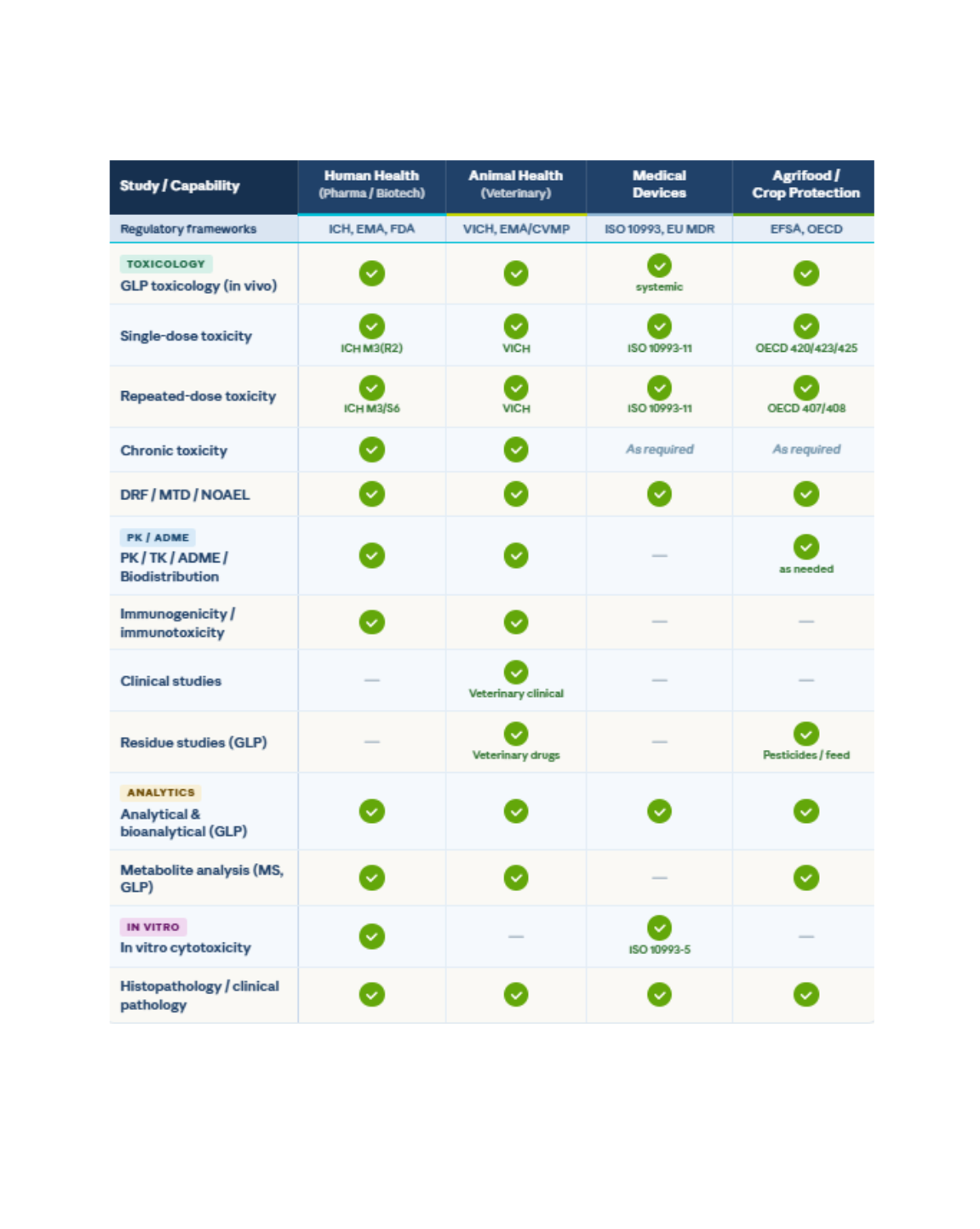
Médicaments à usage humain
Médicaments vétérinaires Lignes directrices
Nouveaux Aliments, ingrédients alimentaires, additifs pour l'alimentation animale, pesticides, autres solutions pour les cultures et substances bioactives pour les soumissions EFSA
Nos services couvrent l'intégralité du flux de travail, de la conception de l'étude à l'archivage final, en combinant :
Nous vous accompagnons tout au long du cycle de vie non clinique :
Conception de l'étude → développement du protocole → exécution → AQ & rapport → archivage
Le tableau récapitule tous les types d'études, combinant les évaluations transversales avec les études spécifiques à l'item et à l'hôte.

CER Groupe réalise des études de toxicologie, de sécurité et des études cliniques pour les médicaments vétérinaires, en parfaite conformité avec les exigences de la VICH et du CVMP.

CER Groupe réalise des études de toxicologie, de sécurité et de PK/TK pour des produits pharmaceutiques, en stricte conformité avec les exigences internationales de l’ICH.
CER Groupe accompagne les fabricants de dispositifs médicaux dans les études d’évaluation biologique, en conformité avec la norme ISO 10993 et le MDR.

CER Groupe réalise des études de toxicologie pour les secteurs de l’agroalimentaire et de l’agriculture, garantissant la sécurité et la conformité réglementaire.
En complément des études animales, CER Groupe propose des services analytiques BPL autonomes, couvrant un large éventail de contextes réglementaires.

Applicable à :

Technologies
Entièrement conforme aux BPL de l'OCDE et aux lignes directrices réglementaires pour les métabolites dans les contextes de la santé humaine, vétérinaire et agroalimentaire.
CER Groupe intègre des techniques de surveillance complètes adaptées à vos objectifs d'étude – garantissant la détection précoce des effets indésirables et une interprétation toxicologique fiable.
Ces paramètres contribuent à la détection précoce des effets indésirables, à une meilleure interprétation toxicologique et à une évaluation bénéfice-risque plus solide.
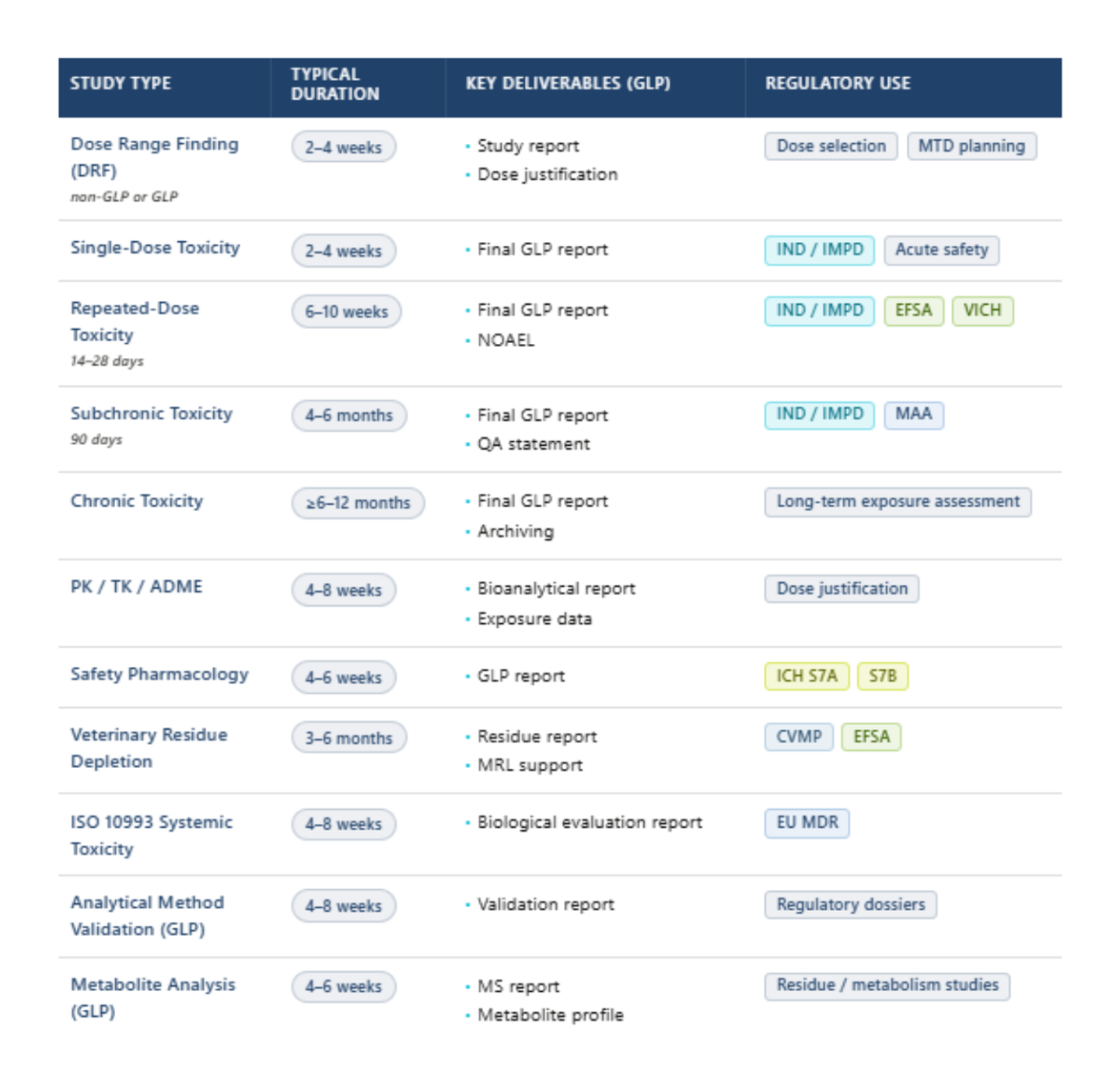
Les délais indicatifs peuvent varier en fonction du type de produit, de la conception de l'étude, de l'espèce et des exigences réglementaires
8 à 12 semaines de l'accord d'étude à la première administration (BPL) – des délais plus courts sont disponibles pour les études analytiques uniquement ou les études exploratoires non-BPL.
